
量子与彩虹
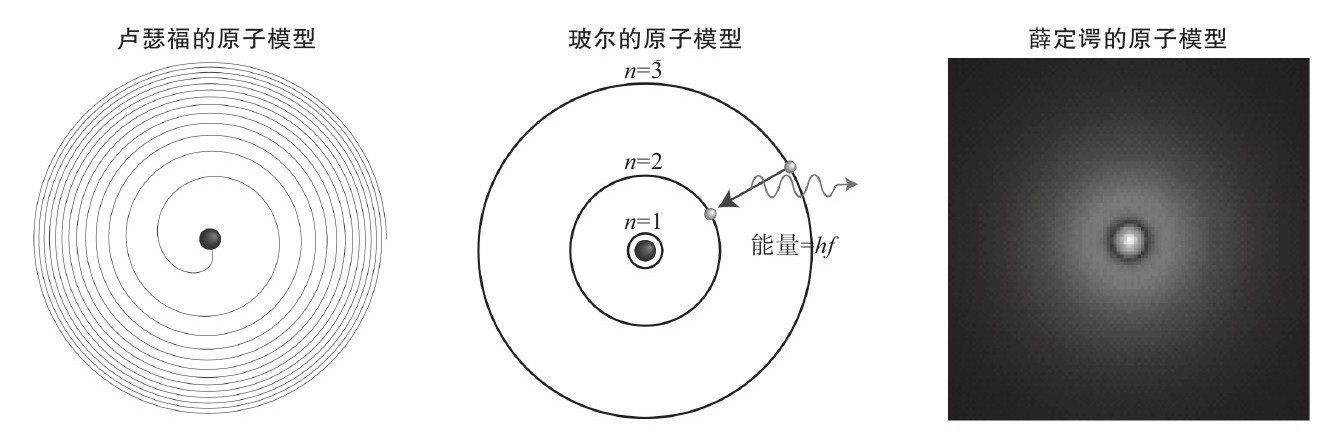
1913年,为了解释原子的机制,丹麦物理学家尼尔斯·玻尔想出了一个激进的念头。他想:也许,不只物质和光是一份一份的(也就是由积木一样的基本构件组成),运动也是如此。有没有可能,运动并不是连续的,而是跳跃的,就像电子游戏“吃豆人”(Pac-Man)或者卓别林的老电影一样,帧与帧之间的切换十分突兀。图6-5中展示了玻尔的原子模型——只有满足某些神秘尺度的圆形轨道才允许存在。最小的轨道被标记为n=1,接着,更大一点的轨道为n=2,以此类推,每个轨道的半径都是最小半径的n2倍[22]。
玻尔的原子模型的第一个也是最重要的一个成就在于,它不会像左边的经典模型那样坍缩。当电子处在最里面的轨道时,它就不可能再向内跃迁了,因为里面没有可用的轨道。不止如此,玻尔的模型还能解释更多事情。较高轨道所具有的能量大于较低的轨道,由于总能量是守恒的,所以,每当电子像吃豆人一样跃迁到较低的轨道时,原子就将多余的能量以一个光子的形式释放出来(见图6-5);如果电子要跳回原来的较高轨道,它又必须付出一定的代价——吸收一个具有所需能量的光子。由于轨道能量是一组离散的数字,这意味着原子只能释放或吸收具有特定能量值的光子。也就是说,一个原子只能吸收或释放具有特定频率的光子。
这解决了一个困扰多年的谜——阳光所形成的彩虹(见图1-5)中,在特定的频率存在着一些神秘的黑线(也就是缺失了某些特定的颜色)。还有,人们在实验室里研究炙热的气体时,观察到每种原子都只能释放和吸收某些特定频率的光,形成独特的光谱特征,就像人的指纹一样。玻尔的原子模型不仅解释了这些光谱线的存在,还解释了氢原子所对应的那个特别的频率[23]。
这是一个好消息,为玻尔赢得了诺贝尔奖(本章中我提到的大多数科学家都获得了诺贝尔奖)。但是,我们不能忽略那个暗潮涌动的坏消息:玻尔的模型只对氢原子有效,而无法解释其他原子,除非它们只剩一个电子。







本书评论