重度和轻度神经认知障碍的类型
根据病因,神经认知障碍可分为几种类型。DSM-5建议将重度或轻度神经认知障碍依据医学或者物质/药物诱导的成因分类。最常见的是阿尔茨海默病,多达三分之二的神经认知障碍都是它造成的(Gatz, 2007)。血管疾病(如脑梗塞或脑血渗漏,俗称中风)、创伤性脑损伤、进行性疾病如帕金森氏病和艾滋病、长期物质滥用都会导致神经认知障碍。
阿尔茨海默病导致的神经认知障碍
患有阿尔茨海默病(Alzheimer's disease, 又译阿尔采末病、老年痴呆症)所致的神经认知障碍的人符合重度或轻度神经认知障碍的诊断标准,学习和记忆有明显衰退。这种病一般开始时只有轻微的记忆丧失,但是随着病情加重,记忆丧失和定向障碍迅速加重。约三分之二的阿尔茨海默病患者表现出精神病症状,包括激越、易激惹、冷漠和烦躁。对阿尔茨海默病人的照料者来说,这些情绪和行为症状通常与认知障碍症状一样难以应对。随着病情恶化,患者可能会变得暴力,并产生幻觉和妄想。阿尔茨海默病多在65岁后发病,但是有一种早发性阿尔茨海默病,比晚发性阿尔茨海默病的病情发展更为迅速(Gatz, 2007)。有阿尔茨海默病的人平均在确诊后8~10年内病逝,通常死于身体机能衰退或者其他不相关的老年期常见疾病,如心脏病。
阿尔茨海默病的脑部异常 阿洛伊斯·阿尔茨海默(Alois Alzheimer)于1906年首次描述了这种疾病,我们现在称为阿尔茨海默病。他发现一位51岁的女病人有严重的记忆丧失和定向障碍。这名妇女55岁时死亡,尸检发现她脑部神经细胞内的纤维扭曲并缠结在一起。这些神经元纤维缠结(neurofibrillary tangles)在阿尔茨海默病患者中普遍存在,但是在没有神经认知障碍的人群中则很少见(图10.3)。这些缠结由tau蛋白构成,会阻碍营养物质和其他必要供给物通过细胞,最终导致细胞死亡。阿尔茨海默病的另一种脑部异常是斑块(见图10.3)。斑块(plaques)是一类名为β-淀粉样蛋白(beta-amyloid)的蛋白质沉淀物,具有神经毒性,堆积在大脑皮层、海马、杏仁核及其他记忆和认知关键脑区的细胞间隙(Atiya, Hyman, Albert, & Killiany, 2003; Du et al., 2001)。
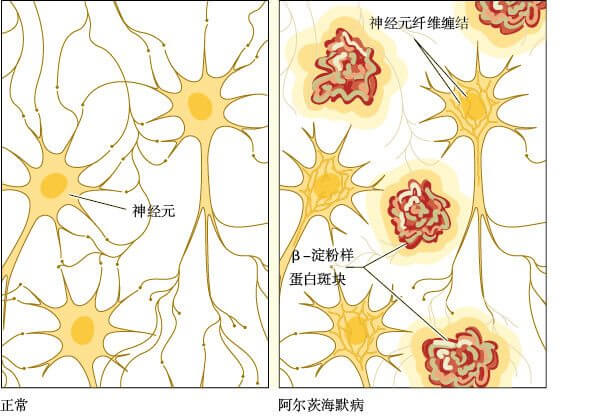
蛋白质沉淀物堆积并造成阿尔茨海默病人脑内神经元纤维缠结和β-淀粉样蛋白斑块。
阿尔茨海默病患者的大脑皮层细胞大量死亡,造成大脑皮层萎缩和脑室扩张(图10.4)。残存的神经元失去了大量树突——将神经元彼此连接起来的枝状突起(图10.5)。这些脑部异常的后果是严重的记忆丧失和自理及其他日常活动协调能力的丧失。
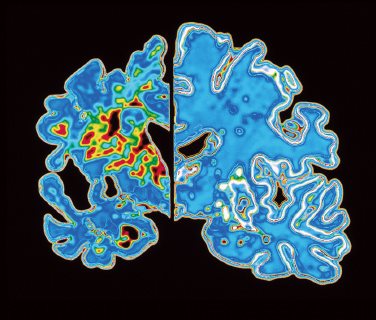
细胞死亡导致晚期阿尔茨海默病人大脑皮层萎缩(左侧;与右侧健康大脑比较)。
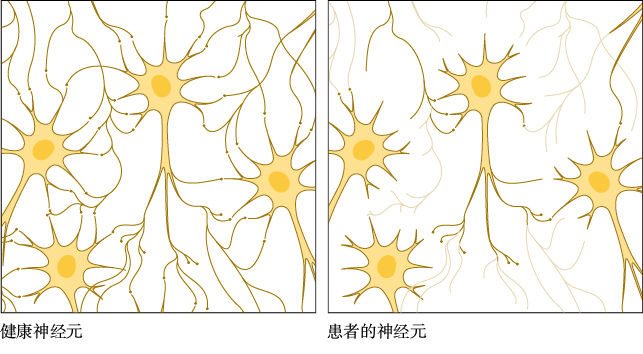
在阿尔茨海默病人的脑中,神经元失去连接彼此的树突。
阿尔茨海默病的病因 遗传因素似乎使一些人更易出现阿尔茨海默病中常见的脑部变化。家族病史研究指出,阿尔茨海默病患者的一级亲属中有24%~49%的人最终出现这种疾病(Gatz, 2007)。与没有该疾病家族史的人相比,具有该疾病家族史的人的终生患病率要高出1.8~4.0倍。双生子研究证实,遗传对阿尔茨海默病及其他类型的神经认知障碍的患病风险有重要影响。对于所有类型的神经认知障碍,同卵双生子的同病率在男性当中是44%,女性当中是58%;异卵双生子的同病率在男性当中是25%,女性当中是45%(Gatz et al., 2006)。
有几种基因与阿尔茨海默病有关。与该病最有关的是19条染色体上的载脂蛋白E基因(ApoE)。该基因调节ApoE蛋白质,而该蛋白质参与经血液运送胆固醇的过程。ApoE还与β-淀粉样蛋白结合,并且可能在后者的调节中起作用。ApoE基因具有三种等位基因或变种:e2、e3和e4。与没有遗传e4等位基因的人相比,从父母一方遗传了e4的人罹患阿尔茨海默病的风险要高2~4倍,从父母双方遗传了双重e4的人患此病的风险要高8~12倍(Coon et al., 2007)。
神经成像研究显示,与不具有e4型ApoE基因的人相比,具有该基因的个体大脑皮层和海马体积更小,甚至在儿童或青少年期也是如此(Jack et al., 2007; Shaw et al., 2007; Thompson et al., 2004)。成年时,具有e4型ApoE基因的人表现出更严重的认知缺陷,阿尔茨海默病的起病时间也更早(Perneczky, Alexopoulos, Wagenpfeil, & Kurz, 2012)。
还有一些基因与不太常见的阿尔茨海默病有关,它们通常在中年发病,且具有较强的家族遗传性。其中一种基因位于21条染色体上(Webb & Murphy, 2012)。关于该染色体上的基因缺陷可能与阿尔茨海默病有关的最早线索来自于这样一个事实:有唐氏综合征的人晚年出现阿尔茨海默病的概率高于一般人群。研究人员推测,造成某些阿尔茨海默病的基因可能位于21条染色体上,唐氏综合征患者更易患上阿尔茨海默病,因为他们多了一条21条染色体。
对阿尔茨海默病高发家族的研究支持这一假设。这些研究已经发现这一疾病与21条染色体上的异常基因有关(Webb & Murphy, 2012)。此外,与这一异常基因相邻的另一基因与淀粉样蛋白前体的生成有关,即淀粉样前体蛋白基因或APP基因。21条染色体该部分的异常可能造成了脑中淀粉样蛋白的生成和积累异常,从而导致阿尔茨海默病。还有很多基因与阿尔茨海默病有关,但研究结果并不一致(Gatz, 2007)。然而,总体来说,与阿尔茨海默病有关的基因也只能解释大约50%的病例。
阿尔茨海默病人的一些神经递质也不足,包括乙酰胆碱、去甲肾上腺素、5–羟色胺、生长激素抑制素(一种促肾上腺皮质激素释放因子)和多肽Y(Micheau & Marighetto, 2011)。乙酰胆碱缺乏尤其值得注意,因为有人认为这一神经递质对记忆功能非常重要。阿尔茨海默病患者的认知功能衰退与乙酰胆碱的不足显着相关(Micheau & Marighetto, 2011)。提升乙酰胆碱水平的药物可以延缓某些阿尔茨海默病患者的认知衰退速度。
在今后几年,我们有可能更深入地了解阿尔茨海默病的致病机理。研究这一疾病的遗传和神经过程的技术正在迅猛发展,探索该疾病的研究者也为数众多。美国有450万阿尔茨海默病的确诊病例,全世界的患病人数为1 800万,而该数字到2050年预期将至少增加三倍(Hebert et al., 2003; Tariot, 2003)。到2050年美国每年用于照料神经认知障碍病人的费用预计将达到4 000亿美元(Lyketsos & Miller, 2012)。希望到那时,我们对这种疾病有足够的了解,可以对其进行有效的治疗。
血管性神经认知障碍
另一种常见的神经认知障碍是血管性神经认知障碍(vascular NCD)。根据认知症状和机能衰退的严重程度,患有此障碍的人符合重度或轻度神经认知障碍的诊断标准。最突出的认知症状是加工速度、注意能力和前面提及的执行功能的明显下降。此外,必须要有近期血管或脑血管疾病的证据。当大脑某些区域供血堵塞使脑组织受损时,脑血管疾病(cerebrovascular disease)就发生了。神经成像技术(如PET和MRI)能检测出脑组织损坏和血流量减少的区域,以确认脑血管疾病。
血流堵塞或者出血引起某一脑区突发性的损伤称为中风(stroke)。血管性神经认知障碍可发生于一次大面积的中风或几次累积的小中风之后。高血压和阻碍脑血流的动脉脂肪堆积也会引发脑血管疾病。除此之外,使脑部发炎的疾病和头部外伤也可能并发脑血管疾病。

大约25%的中风患者认知缺陷严重到足以做出神经认知障碍诊断(Stephens et al., 2004)。年龄较大(超过80岁)、受教育程度低、有中风病史或有糖尿病的中风病人更可能患血管性神经认知障碍。
即使那些没有立即出现神经认知障碍的中风患者,与没有中风的同龄人相比,前者认知衰退的风险也更高(Hachinski, 2008)。最终很可能出现神经认知障碍的中风病人一般在随后时间内更易中风,其中有些症状比较明显,有些则是“无声的”(或没有明显症状),只有过后才能发现。此外,患有痉挛、心律失常、充血性心力衰竭和肺炎等可能引发广泛缺氧或供血不足病症的病人,也更可能出现血管性神经认知障碍(Hachinski, 2008)。
与其他疾病有关的神经认知障碍
很多重大疾病都会导致神经认知障碍,包括路易体病、帕金森氏病、艾滋病和亨廷顿病。帕金森氏病是一种退行性大脑障碍,在一般人群中的发病率约0.3%,在60岁以上人群中的发病率为1%(Samii, Nutt, & Ransom, 2004)。阿里(Muhammed Ali)和福克斯是两位有帕金森氏病的名人。该病主要症状为颤抖、肌肉僵硬和不能发起运动。这些症状是由于制造神经递质多巴胺的脑细胞死亡引起的。约75%的帕金森氏病患者会出现神经认知障碍(Aarsland & Kurz, 2009)。
因路易体疾病所致的神经认知障碍是仅次于阿尔茨海默病最常见的进行性神经认知障碍。它是由脑中生长的一些异常的圆形结构造成的。它的典型症状是注意与警觉的变化、视幻觉以及帕金森氏病的症状。有些证据表明它与阿尔茨海默病和帕金森氏病有关。
艾滋病会引起轻度或重度神经认知障碍,记忆和注意力受损。艾滋病人的心理过程变得缓慢——他们可能难以跟上谈话,或需要更长时间组织自己的想法和完成一些简单而熟悉的任务。他们可能会回避社交,失去自发性。四肢无力、行动笨拙、失去平衡能力以及缺乏协调性也很普遍。如果神经认知障碍进一步发展,这些缺陷会变得更加严重。言语能力受损越来越严重,对语言的理解力亦是如此。他们只能卧床,通常对周围的事物漠不关心。
与艾滋病有关的重度神经认知障碍的诊断是在缺陷和症状变得严重而全面、日常活动和机能遭到严重破坏时做出的。随着抗逆转录病毒治疗广泛用于治疗艾滋病,相关的神经认知障碍新增病患数和严重程度都下降了。另一方面,由于这些药物让更多艾滋病人存活更长时间,相关的神经认知障碍患者的数量在增加,特别是在药物滥用或丙型肝炎感染人群中(Nath et al., 2008)。
亨廷顿病是一种罕见的遗传性障碍,发病较早,通常在25~55岁之间。这类患者最终会出现重度神经认知障碍和舞蹈症——无规律的抽搐、面部扭曲和痉挛。亨廷顿氏症通过第4条染色体上的单一显性基因遗传(Gusella, MacDonald, Ambrose, & Duyao, 1993)。如果父母一方携带此基因,那么子女有50%的可能性遗传该基因并发生此病症。亨廷顿病影响大脑中的多种神经递质,但目前尚不清楚哪些变化会导致舞蹈症和神经认知障碍。
轻度和重度神经认知障碍的病因还包括另外一种罕见的疾病——朊病毒病(也称克雅二氏症)、脑肿瘤、内分泌疾病(如甲状腺机能减退)、营养不良(如缺乏维生素B1、烟酸和维生素B12)、感染(如梅毒)和其他神经疾病(如多发性硬化)。此外,长期大量饮酒、滥用吸入剂和镇静剂,特别是在营养不良的情况下,也会引发脑损伤和神经认知障碍。多达10%的长期酗酒者可能出现神经认知障碍(Winger, Hofmann, & Woods, 1992)。酗酒引发的神经认知障碍往往发病缓慢、隐秘。虽然补充营养可以减缓发病,但是这种障碍一般是持续的,尤其是长期饮酒或年龄增大时。
创伤性脑损伤是神经认知障碍的另一个潜在病因。脑损伤可以是枪击等穿透性伤害或闭合性脑外伤,后者通常是对头部的撞击和/或冲击力造成的,例如机动车交通事故,爆炸,或运动损伤。在美国的脑损伤病例中摔倒占28%,机动车事故占20%,被物体击中占19%,暴力占11%,自行车事故占3%(Langlois, Rutland-Brown, & Wald, 2006)。下述案例中的利兰在经历机动车事故后出现了重度神经认知障碍。
个案研究
41岁的工人利兰一天夜里下班后正行驶在回家的乡村公路上。一个醉酒司机驾车闯过停车标志,猛烈地撞到利兰车子的驾驶位一侧。利兰没有系安全带。猛烈的撞击将他抛出挡风玻璃,甩到了人行道上。他保住了性命,但是头部严重受伤,还有多处骨折和伤口。利兰昏迷了两个多星期,然后在医院住了两个月的时间养伤。
回家以后,他似乎变成了另一个人。出事以前他热爱家庭、安分守已,有很强的幽默感。车祸之后,利兰变得郁闷而易怒。因为琐事便对妻子和孩子们大喊大叫。有一次当利兰的妻子因为他辱骂孩子们而表示不满时,他甚至掌掴了妻子。
利兰工作上的表现也好不到哪里去。他发现自己很难集中精神工作,不能遵循老板的指示。当老板找他谈他未能正常工作的问题时,利兰表达不出多少他正在经历的困境。他很生老板的气,指责他想解雇自己。利兰的同事们以前一直很喜欢他,并且欢迎他在事故后重返工作岗位,但是利兰不久就开始对他们发脾气,就像他对妻子和孩子们发脾气一样。他指责好朋友偷了他的东西。这些激烈的症状持续了大约3个月。逐渐地,症状开始减轻。车祸发生18个月后,利兰的情绪和人格似乎回归正常。他的认知能力也有了很大的改进,但是他发现与事故发生前相比,他仍然难以集中注意力和完成任务。
利兰的症状正是严重的创伤性脑损伤(traumatic brain injury)之人的典型特征。他的认知能力、情绪和人格都有所变化。幸运的是,利兰的症状在几个月后逐渐减轻。许多中度到重度的脑损伤患者永远不能完全康复(Beatty, 1995)。
单次闭合性头部损伤引起的神经认知障碍一般是轻度的,而且与诸如拳击手、一些士兵或经历多次车祸的人所承受的反复闭合性头部损伤所造成的神经认知障碍相比,更可能随着时间推移而消失。美国每年有160~380万起创伤性脑损伤事件是由体育和娱乐活动造成的;年轻人最可能因为头部损伤而出现神经认知障碍,因为他们比其他人群更可能参与导致头部外伤的风险活动(CDC, 2007)。
在伊拉克和阿富汗服役的士兵由于路边炸弹和其他引爆装置导致的爆炸,出现创伤性脑损伤的比率也很高。据估计,这些战争的所有伤害中,22%是创伤性脑损伤(Committee on Gulf War and Health, 2008)。创伤性脑损伤的士兵会出现与神经认知障碍类似的神经认知功能下降,以及抑郁、攻击行为、长期失业和社会关系问题。







本书评论