
第7章 恒星的化学指纹
“一闪一闪亮晶晶,满天都是小星星!”
1859年,罗伯特·本生(Robert Bunsen)和古斯塔夫·基尔霍夫(Gustav Kirchhoff)公布了轰动性发现,由此打开了一个全新的科学世界。本生激动地向同事宣布:
我和基尔霍夫正在合作的研究工作,让我们睡不着觉……基尔霍夫有了一个美妙的发现,一个完全出乎预料的发现,他知道太阳光谱里的暗线是怎么来的了……这下好了,我们有办法确定太阳和其他恒星(见图7-1)的化学成分了,和我们用化学试剂去测定硫酸、氯等物质的化学成分一样准确。我们还能用这个方法确定地球的化学成分,就像确定太阳的化学成分那么容易,比如说,我能在20克海水里检测到锂。

化学指纹
本生和基尔霍夫发现,每种化学元素都有独特的指纹,循着这些指纹,他们就能找到元素的踪迹。把一种元素放到火上燃烧,它会发出特定颜色的光,让这束光透过棱镜,我们就会在一系列特定的波长处看到清晰、明亮的谱线。以金属钠为例,它燃烧后会发出明亮的黄光。我们在路上看到有许多路灯都发出黄色的光,就是因为灯里有钠蒸汽。用棱镜把钠发出的光分解成光谱,我们会在光谱的黄光区域看到一对锐利的谱线,这就是钠的化学指纹,它暴露了钠的踪迹。本生和基尔霍夫把元素逐一放到火上燃烧,再用棱镜分解它们发出的光,然后把它们的独特谱线一一记录下来。或许,你还记得在化学实验课上见过的本生灯,那就是本生发明的。
宇宙条形码
像恒星这样炽热的物体,它发出的光是其表层粒子随机碰撞产生的,遍布所有的波长,所以经过棱镜分解后,我们会看到一段连续的光谱。如果恒星的大气里有某种元素,这种元素就会在特定的波长处吸收恒星发出的光,恒星的光谱在相应的波长处就会因为缺少光而形成暗线(即吸收谱线)。本生和基尔霍夫把这些暗线与在实验室里燃烧这种元素得到的明亮谱线进行比对,发现两者的波长竟然完全一样。通过这种方法,他们就能知道恒星的大气是否含有这种元素了。然而,他们当时并不知道这种方法背后的原理,因为还要等上半个多世纪,人们才弄明白原子是如何与光相互作用的,不过没关系,这种方法在当时照样很管用。
恒星的光谱如同商品的条形码,精确地记录着恒星的化学成分。本生和基尔霍夫把恒星光谱中的暗线,与他们在实验室里看到的明亮谱线对比之后,就能识别出恒星含有哪些化学元素。即使恒星远在数万亿公里之外,我们也能清楚地看到每种元素的化学指纹。图7-2由上至下依次展示了太阳的光谱和钠、氢、锂、汞四种元素的发射光谱。太阳光谱里的暗线与钠和氢的发射谱线一一对应,却与锂和汞的谱线对不上,清楚地表明了太阳的大气中有钠和氢,没有锂和汞。

想当初,本生和基尔霍夫用这种方法第一次确定了恒星的化学组成时,他们该有多么惊讶啊!
原子小金刚
1913年,尼尔斯·玻尔建立了一个原子模型,让电子在一系列固定能级的轨道上围绕原子核运动,这是人类在认识自然的过程中所取得的又一项重大突破。我们现在知道这个模型是可行的,因为电子具有波动性,在围着原子核转圈的同时还不会互相重叠,只有具有特定波长的波才能做到。玻尔能用他的模型解释原子光谱里的谱线是怎么产生的。当一个电子从高能级跃迁到低能级,就会放出一个光子,光子的能量正好等于两个能级的能量差(见图7-3中邮票上的公式)。电子只能待在一系列离散的能级上,所以它只能放出具有特定能量(颜色)的光子,本生和基尔霍夫在实验室里看到的元素的特征谱线就是这么来的。

玻尔的原子模型取得了非常大的成功,玻尔也凭此获得了1922年的诺贝尔物理学奖。尽管如此,玻尔觉得他的模型还能做更多的事。如果这个模型真实地反映了原子的结构,它应该能解释诸如原子在化学反应中是怎么互相结合的,为什么每种原子都有自己独特的化学性质等问题。玻尔经过一番研究,取得了一些进展,但最终还是不得不认输。后来,还是奥地利的一位天才青年沃尔夫冈·泡利(Wolfgang Pauli),设法解决了玻尔没能解决的问题。年仅19岁的泡利就以相对论为题写了一篇论文,并一举成名。
一山不容二虎
1925年,泡利想出了解决办法。质子和电子虽然电量相同,但电性相反(质子带正电,电子带负电)。如果原子呈电中性,那么原子核外有多少个电子,原子核里就要有同样多的质子才行。在玻尔的原子模型里,电子全都待在最低的能级上。若实际情况真是如此,那就很难用他的模型解释原子的化学性质了。于是,泡利就想到让电子行为乖张一些,只有这样才能解决这个难题。他提出,一个量子态上只能容纳一个电子,就好比一个停车位要么空着,要么最多只能停放一辆车,这就是泡利不相容原理。
根据不相容原理,一个能量上究竟能容纳多少个电子,取决于它有多少个“停车位”,化学家把这些“停车位”组合称为电子层。量子力学能够计算出每一层可容纳的电子数,比如,第一层最多可容纳2个电子,第二层8个电子,第三层8个电子,第四层18个电子等。氢原子只有1个电子,这个电子就待在能量最低的第一层上。氦原子有2个电子,它们也都待在第一层,这样一来,第一层的两个“停车位”就被填满了。锂原子有3个电子,其中2个电子填满第一层,第3个电子就只能待在第二层了。图7-4展示了这些原子还有更多原子的电子排布情况。电子就是这样一步步地把每一层填满,每个电子只能占据一个空位。
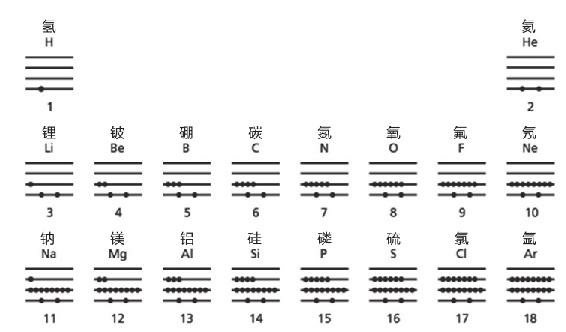
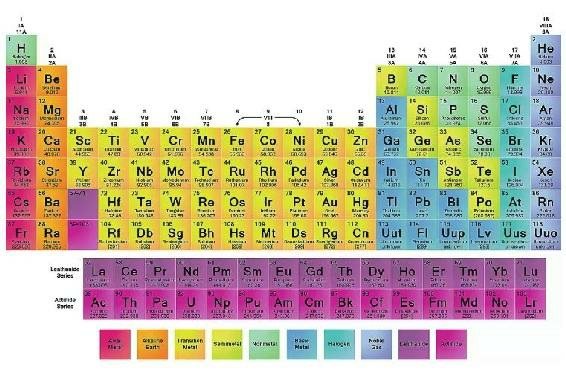
泡利认为,只有最外层的电子——未被填满的最高能量层上的电子——参与化学反应。正是这些电子决定了元素的化学性质。不同种类的原子,只要最外层的电子数相同,就会表现出相似的化学性质,这也解释了为什么化学元素周期表蕴含着重要的化学信息。举例来说,钠(Na)和钾(K)之所以具有相似的化学性质,就是因为它们的最外层(钠的最外层是第三层,钾的是第四层)都有1个电子,这也是它们都出现在元素周期表的第一列的原因(见图7-5)。1945年,泡利因为这项成就获得诺贝尔物理学奖。
自旋与统计
依据基本粒子的行为特征,我们可以把它们分成两类:一类遵从泡利不相容原理,是构成物质的基本粒子,比如电子、质子、中子和夸克;另一类是光子和负责产生作用力的交换粒子,它们不受不相容原理的约束。一种粒子究竟属于上面哪一类,全由它的奇特属性——自旋——说了算!沃尔夫冈·泡利(见图7-6)为基础物理研究做出了许多重要贡献,给出电子自旋的数学描述并证明自旋——统计定理就是其中一项贡献。在第8章里,我们将详细讲述粒子与它们的作用力。
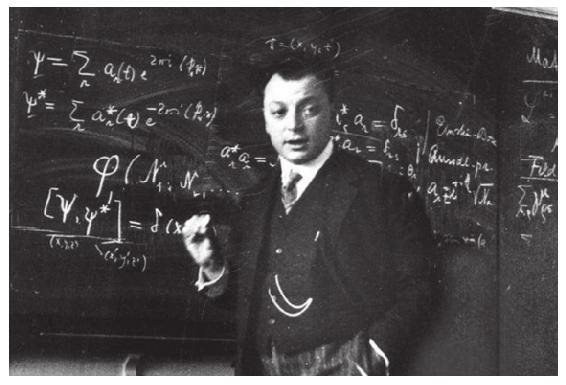







本书评论